A kromatográfia története a XIX. század közepére nyúlik vissza. A kromatográfia nevét a XX. század első évtizedében kapta, Mihail Szemjonovics Cvettől, aki elsősorban növényi pigmentek, például klorofill elválasztásával kezdte meg a kromatográfiás technikák kidolgozását. Az azóta eltelt idő során kifejlesztett új kromatográfiás módszerek és mérőberendezések napjainkra az analitikai kémiai feladatok roppant széles körének megoldására tették alkalmassá a kromatográfiás technikákat.
Az ionkromatográfia olyan nagyhatékonyságú analitikai módszer, melynél az ionok elválasztása az álló- és a mozgófázis közötti ioncsere-egyensúlyon alapul. A mai modern kromatográfiás rendszerekhez hasonlóan az ionkromatográfia technikai megvalósítása oszlop alkalmazásával főként elúciós, illetve ritkábban kiszorításos analízis segítségével történik. Az ionkromatográfia mind elvét, mind technikai megvalósítását tekintve a folyadékkromatográfiás módszerek családjába sorolható, attól inkább csak történeti okokból szokás megkülönböztetni. Ma a szakirodalomban az ionkromatográfiát különbözőképpen definiálják, tágabb értelemben minden olyan módszer ide sorolható, ami ionok kromatográfiás elveken nyugvó meghatározását jelenti. Az ionpár kromatográfia és a peptidek meghatározásának különböző lehetőségei is elvben ide sorolhatók lennének. A gyakorlatban viszont inkább a vízoldható ionok, illetve ionizálható vegyületek ioncsere-egyensúlyon alapuló meghatározását értik ionkromatográfia alatt, ahol tipikusan vezetőképesség-mérésen alapuló detektálást alkalmaznak.
A modern ionkromatográfia a folyadékkromatográfiás technika fejlődése révén az 1970-es években született meg. A korábban alkalmazott spektrofotometriás detektálást felváltó vezetőképesség mérésén alapuló detektor és a nagyhatékonyságú folyadékkromatográfiás töltetek mintájára kialakított ioncserélő oszlopok alkalmazásával megszületett az ionkromatográf, melynek segítségével az 1980-as évekre lehetővé vált a kationok és anionok kicsiny koncentrációban (ppm szinten) történő meghatározása.
Egy mai modern ionkromatográf felépítése gyakorlatilag megegyezik a HPLC felépítésével, azaz az alábbi fontos egységekből áll:
eluens tároló edények
pumpa
adagoló
kolonna
detektor
A működés folyamán az eluenstárolóban elhelyezett mozgófázist az ún. alternáló mozgást végző dugattyús pumpa (ún. reciprok pumpa) továbbítja; a) az eluens átáramlik az adagolón, mely során a mintatartó hurokból magával ragadja a mintát és eljuttatja az oszlopra; b) az oszlopon megtörténik az ionok elválasztása, c) majd a detektor valamely fizikai vagy kémiai tulajdonság mérésén keresztül a mintát alkotó ionok koncentrációjával arányos jelet állít elő, melyet d) átalakítást követően általában egy adatfeldolgozó szoftverrel ellátott személyi számítógép jelenít meg, azaz megszületik a kromatogram, amint azt az alábbi animáció is szemlélteti.
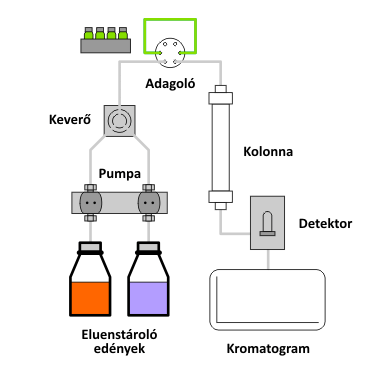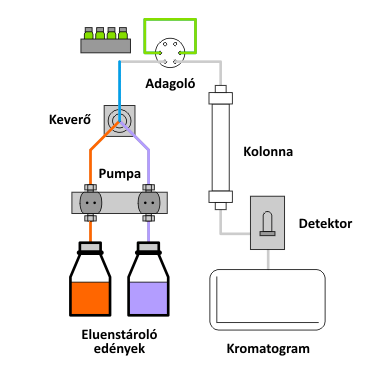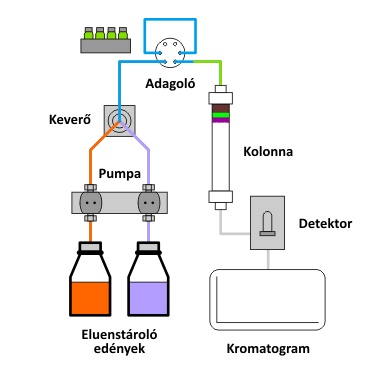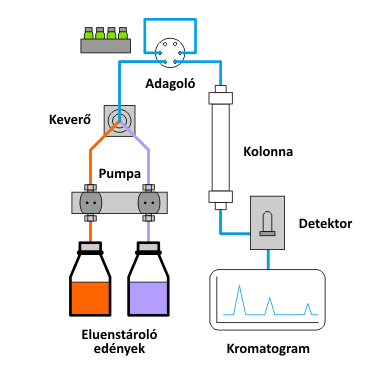
Az ionkromatográf felépítése
Amint korábban említettük, az ionkromatográf működését, illetve felépítését tekintve gyakorlatilag megegyezik a HPLC készülékkel, melyet korábbi tanulmányaik során megismertek. Ennek megfelelően, itt csak egyetlen fontos elemét ismertetjük, az eluens továbbításáért felelős ún. alternáló mozgás végző dugattyús pumpát. A pumpa feladata a mozgófázis folyamatos szállítása. Ezt a feladatot igen nagy nyomáson (max. 400 bar) pulzálásmentesen, stabil és szabályozható áramlási sebesség biztosítása mellett kellett megoldani. Erre több műszaki megoldás is született, amelyek közül a gyakorlatban az alábbi animáción látható kialakítás (reciprocating pump) terjedt el.
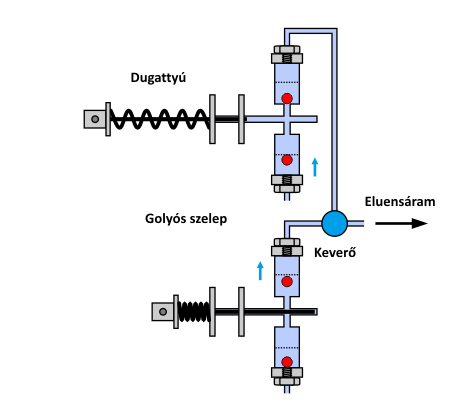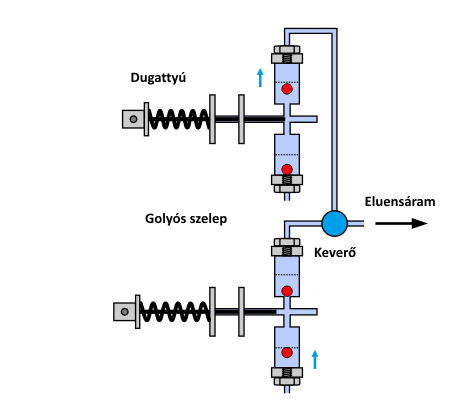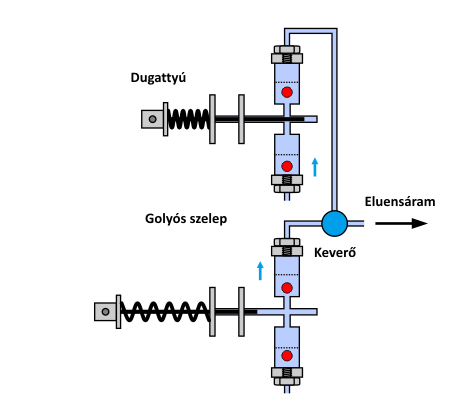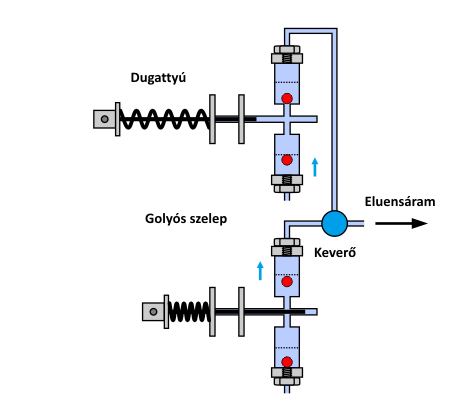
A HPLC pumpák legelterjedtebb változatának működési elve
A kis dugattyú-térfogatú, alternáló mozgást végző pumpa két, egymással ellentétes ütemben működő pumpafejből áll. A két fej sorba kötésével és fáziseltolásával, azaz a szállítási ciklusok megfelelő átlapolásával lehetővé válik a folyamatos térfogatáram kialakítása.
Az ioncsere kromatográfia (ion exchange chromatography) állófázisként ioncserélő tulajdonságú anyagokat használ a tipikusan állandó töltéssel rendelkező vegyületek (pl. erős savak és bázisok, szervetlen ionok) meghatározására. Az elválasztás az egyes ionok és az állófázison elhelyezkedő ellentétes töltésű funkciós csoportok között kialakuló kölcsönhatáson alapul.
Az állófázisként alkalmazott ioncserélőket csoportosíthatjuk
töltésük szerint:
anioncserélők: pozitív töltésű funkciós csoportokkal rendelkeznek (pl. protonált aminocsoport, kvaterner amin)
kationcserélők: negatív töltésű funkciós csoportokkal rendelkeznek (pl. deprotonált szulfonsav, karboxilcsoport)
töltésük pH-függése szerint:
erős ioncserélő: ioncsere kapacitása független a pH-tól (pl. kvaterner amin, szolfonsav)
gyenge ioncserélő: ioncsere kapacitása pH függő (egyéb aminocsoportok, karboxilcsopiortok)
Állófázis hordozóként leggyakrabban megfelelő ioncserélő funkciós csoportokkal ellátott térhálósított műgyantát (pl. sztirol és divinil-benzol kopolimer) vagy szilikagélt alkalmaznak.
Az elválasztást az állófázis illetve a minta töltésének „hangolásával”, azaz az ioncserélő anyagi minőségének és az eluens pH-jának változtatásával lehet befolyásolni. Az ioncsere mechanizmusa a következőképpen írható le:
kationcserélő esetén:
R-(SO3H)n + Mn+ ⇌ R-(SO3-)nMn+ + n H+
anioncserélő esetén:
R-[N(CH3)3OH]n + An- ⇌ R-[N(CH3)3+]nAn- + n OH-
Az oszlop által visszatartott komponensek elúciója megfelelő sav vagy bázis vizes oldatával valósítható meg. Az ioncsere-egyensúlyon alapuló elválasztás mechanizmusát egy kationcserélő oszlop példáján az alábbi animáció mutatja.
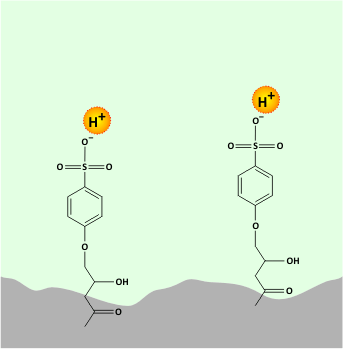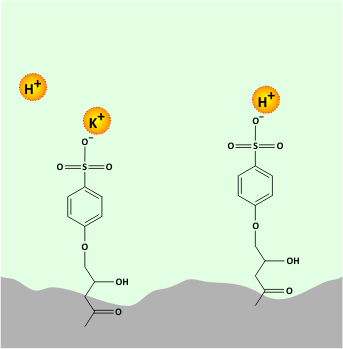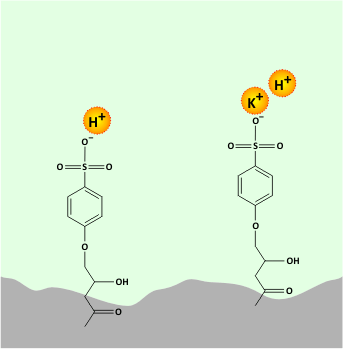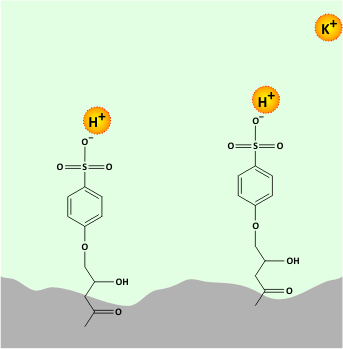
Az ioncsere-egyensúlyon alapuló elválasztás mechanizmusa
Az állófázis felületén kialakított ionos funkciós csoportok (pl. -SO3-) elektrosztatikus kölcsönhatás révén megkötik a minta ellentétes töltésű kationjait, majd az elúció során a mozgófázisban jelenlevő protonok leszorítják az állófázisról a megkötött kationokat.
Az ionkizárásos kromatográfia (ion exclusion chromatography) erős kation illetve anioncserélőket alkalmaz elsősorban kisebb méretű molekulák (pl. kis szénatomszámú karbonsavak, gyenge bázisok, hidrofil vegyületek) elválasztására. Érdekessége, hogy a korábban bemutatott ioncsere kromatográfiával ellentétében az anionok elválasztására kation-, míg a kationok szeparációjára anioncserélőt alkalmaznak. Ebben az esetben az azonos töltéssel bíró komponens a fellépő elektrosztatikus taszítás miatt nem tud az állófázissal kölcsönhatást kialakítani, azaz számottevő visszatartás nélkül halad át a rendszeren. A megfelelő pH beállításával viszont elérhető, hogy az elválasztani kívánt molekulák semleges (ún. ionvisszaszorított) állapotba kerülve bejuthassanak az állófázis pórusaiba, és a kialakuló kölcsönhatásokon keresztül létrejön az elválasztás.
Apolárisabb minták esetén az ioncserélő gyanta anyagával –amely apoláris tulajdonságú polimer– hidrofób-hidrofób (vagy akár van der Waals) kölcsönhatások kialakulására is lehetőség nyílik.
Az ionkromatográfiás rendszerek fejlesztése során –a sokrétű gyakorlati kihívásoknak megfelelően– különféle módszereket dolgoztak ki az ionok elválasztására. Ezek egyike az ún. ionelnyomásos, vagy más néven kétkolonnás technika. Működésének lényegét a kationok elválasztásán keresztül mutatjuk be. Kationok elválasztása esetén természetesen szükségünk van egy kationcserélő oszlopra, amelynél erős sav híg vizes oldatával nyílik lehetőség a kationok elúciójára. Amint korábban említettük, az ionkromatográfiás módszerek főként vezetőképesség-mérésen alapuló detektálást alkalmaznak. Mivel ennél a kialakításnál az eluens vezetőképessége igen nagy, az eluenst közvetlenül a detektorba vezetve olyan nagy háttér jel képződne, ami nem tenné lehetővé a mintát alkotó ionok által okozott viszonylag kicsiny vezetőképességváltozás detektálását. A mozgófázis vezetőképességének csökkentése érdekében a kationcserélő oszlopról lejövő eleuns áramot (amely tartalmazza az elválasztott kationokat is) rávezetik egy nagy ioncserekapacitású anioncserélő oszlopra (második kolonna). Itt jegyezzük meg, hogy ma erre a célra gyakran nem oszlopot, hanem mikromembrán ionelnyomót vagy ioncserélővel töltött kapillárist használnak. Ez az ún. ionelnyomó oszlop, amely mind a mintából, mind pedig az eluensből származó anionokat hidroxidionokra cseréli. Az így ekvivalens mennyiségben oldatba kerülő hidroxidionok az eluens protonjaival reagálva vizet termelnek, azaz a mozgófázis vezetőképessége lecsökken, ezáltal a mintában eredetileg jelenlevő kationok jól értékelhető jelet adva detektálhatóvá válnak.
1. oszlop: kationcserélő: elválasztás
R-(SO3H)n + Mn+ ⇌ R-(SO3-)nMn+ + n H+
2. oszlop: anioncserélő: ionelnyomás (vezetőképesség csökkentése)
R-[N(CH3)3OH]n + An- + nH+ ⇌ R-[N(CH3)3+]nAn- + n H2O
A kétkolonnás technika sémáját az alábbi ábra mutatja be.
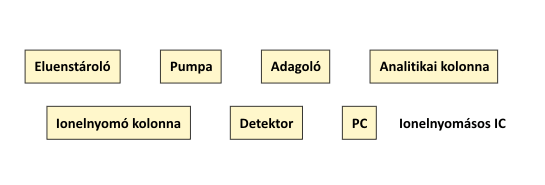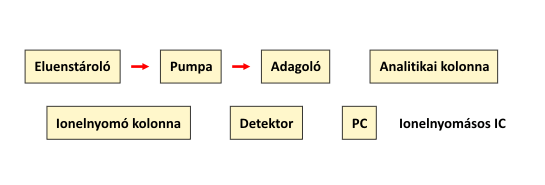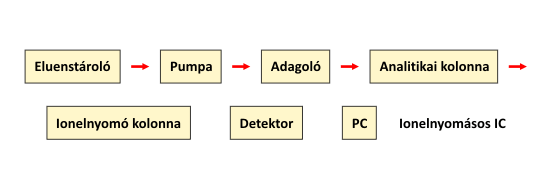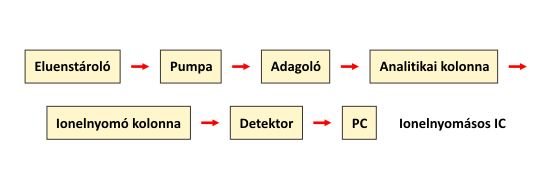
A kétkolonnás technika sémája
Az anionok meghatározása ezzel a technikával anioncserélő kolonna és kationcserélő ionelnyomó oszlop alkalmazásával lehetséges.
Az előzőekben bemutatott kétkolonnás rendszer hátrányai között mindenképpen meg kell említeni, hogy az első kolonnán elválasztott komponensek csúcsai a második oszlopon kiszélesednek, jelentősen rontva ezzel a meghatározás hatékonyságát. Ennek a nemkívánatos jelenségnek az elkerülése az ún. egykolonnás rendszerekkel vált lehetségessé. Az ionkromatográfiás oszlopok fejlesztése során egyre kisebb szemcseméretű és egyre kisebb ioncserekapacitású oszlopok jelentek meg, melyeknél kicsiny vezetőképességet eredményező, elsősorban szerves savakkal illetve sóikkal (pl. ftálsav, benzoesav, borkősav) végezve az elúciót, az eluens közvetlenül, ionelnyomás alkalmazása nélkül bevezethető a detektorba. Ennek ellenére ma az ionelnyomásos rendszerek a gyakoribbak, a fentebb említett korszerű ionelnyomásos megoldások megjelenése miatt (pl. mikromembrán ionelnyomó, stb.).
Az egykolonnás technika sémáját a következő ábra mutatja be.

Az egykolonnás technika sémája
Az ionkromatográfiát a műszeres analitika számos területén alkalmazzák szervetlen és szerves ionok minőségi és mennyiségi meghatározására. A módszer mérési tartományát elsődlegesen az adott rendszerhez kapcsolt detektor határozza meg, általánosságban elmondható, hogy tipikusan ppm koncentrációszinten hajthatók végre a mennyiségi elemzések, melyekre példákat a környezetvédelem, klinikum, gyógyszer- vagy az élelmiszeripar területéről említhetünk.
Mi értünk ionkromatográfia alatt?
Milyen módszerek sorolhatók az ionkromatográfia családjába?
Hogyan épül fel az ionkromatográf?
Mi az ioncsere kromatográfia lényege?
Hogyan csoportosíthatók az ioncserélők?
Mi az ionkizárásos kromatográfia működési elve?
Mit nevezünk kétkolonnás ionkromatográfiának?
Mit nevezünk egykolonnás ionkromatográfiának?
Milyen eluensek használhatók az egykolonnás ionkromatográfia esetében?