A kémiai analízist megelőző mintaelőkészítés során tipikusan két cél elérése vezérli az analitikust: a meghatározandó komponens(ek) koncentrációjának növelése és a minta analízist zavaró komponenseinek eltávolítása. Időnként az oldószercsere is szükséges lehet, azaz a minta oldószerét (leggyakrabban víz) valamilyen más, az analízis megvalósítása szempontjából kedvezőbb oldószerre cseréljük. Ezen célok elérésének leggyakrabban alkalmazott módszere az extrakció. A két, egymással nem elegyedő oldószer érintkeztetésén alapuló hagyományos, nagytérfogatú folyadék-folyadék extrakcióval többször is találkoztak tanulmányaik során, így ennek ismertetésétől itt eltekintünk. A módszer óriási előnye a rendelkezésre álló igen nagy számú oldószer nyújtotta széleskörű alkalmazhatóságban rejlett, azonban számos hátránya miatt már nemigen tudja teljesíteni azokat az elvárásokat, amiket napjainkban fogalmaznak meg egy modern mintaelőkészítési technikával szemben: a nagy oldószer felhasználás miatt nem gazdaságos és nem eléggé környezetbarát, idő- és munkaigényes, nehezen automatizálható, így nem képes nagyszámú minta gyors feldolgozására, sok esetben emulzióképződés vagy habzás teszi nehézkessé (vagy akár lehetetlenné) a fázisok szétválasztását. Nem véletlen tehát, hogy már korábban felmerült az igény olyan új extrakciós technikák kidolgozására, amelyek képesek a felsorolt hátrányok leküzdésére. Az alábbiakban ezen új technikák közül mutatunk be néhány fontosabbat, mégpedig szerves komponensek kinyerésének esetét szem előtt tartva.
A szerves komponensek kinyerésére szolgáló extrakciós technikák közül a szilárdfázisú extrakció (solid phase extraction, SPE) a leggyakrabban alkalmazott mintaelőkészítési eljárás. Az SPE tipikusan félillékony komponensek folyadék halmazállapotú mintákból történő extrakciójára használatos. Amint azt az elnevezés is mutatja ebben az esetben az extraháló fázis szilárd halmazállapotú. Ahhoz, hogy egy ilyen szilárd töltettel a folyadék-folyadék extrakcióval összemérhető hatékonysággal elvégezhető legyen az extrakció művelete, olyan szorbensek kifejlesztésére volt szükség, amelyek igen erősen képesek visszatartani (azaz megkötni) az analizálni kívánt összetevőket. Természetesen a gyors és reprodukálható módon végbemenő szorpció mellett az is elengedhetetlen feltétel, hogy a megkötött komponensek elúciója (azaz leoldása) könnyen és teljes mértékben végbemenjen. A gyakorlati alkalmazhatósághoz az említetteken kívül az is fontos, hogy a szorbens ne tartalmazzon kioldható szennyezőket, jól nedvesedjen a minta mátrixa által, kémiailag inert, stabil és olcsón előállítható legyen. Az SPE modernkori története 1970-es években kezdődött, amikor is a Waters cég a fentiekben leírt tulajdonságokkal rendelkező, műanyag csövecskékbe (oszlopokba) töltött szilikagél alapú tölteteket hozott forgalomba. Az SPE módszer működési elvét az alábbi animáció mutatja.
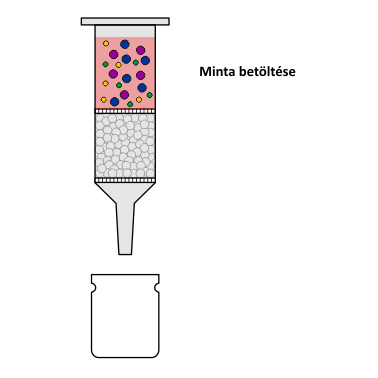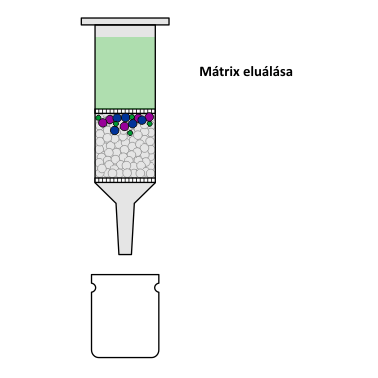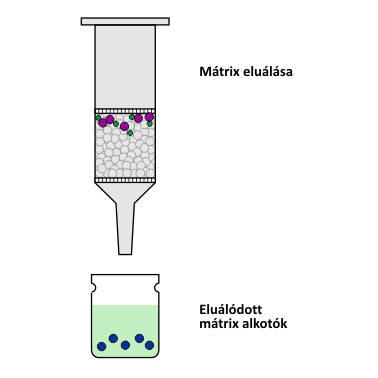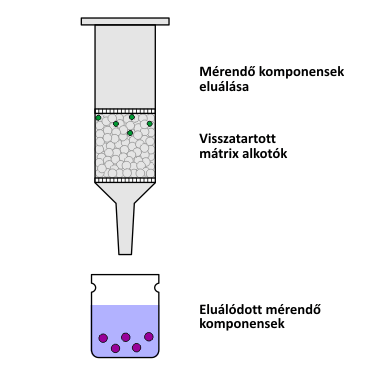
Az SPE módszer működési elve
Az első lépésben az extraháló töltetet kondícionálni kell, azaz alkalmassá kell tenni a minta befogadására, máshogy megfogalmazva biztosítani kell, hogy a minta mátrixa nedvesíteni tudja a töltet anyagát (amint azt korábban említettük, ez elengedhetetlen feltétele a hatékony extrakciónak). Ez lényegében egy megfelelő anyagi minőségű oldószerrel történő öblítést jelent. Mivel általában vizes közegű minták extrakciójához használatos az SPE, a kondícionálás tipikusan metanollal hajtható végre.
A második lépésben következik a minta felvitele. Harmadik lépésben a nemkívánatos szennyezők eltávolítására egy oldószeres öblítést iktatnak be. Az utolsó lépésben pedig egy megfelelően megválasztott oldószerrel leoldják az oszlopon visszatartott komponenseket.
Ahhoz, hogy az SPE a napjainkban tapasztalt mértékben elterjedhessen, a különféle tulajdonságokkal rendelkező vegyületek meghatározásához eltérő szorpciós képességekkel rendelkező tölteteket kellett kifejleszteni, hiszen természetesen nincs olyan univerzális töltet, amely mindenféle komponens, tetszőleges mátrixból történő extrakciójára alkalmas lenne. Mára a HPLC technika állófázisainak mintájára kifejlesztett töltetek számos képviselője kapható, melyek leggyakrabban szilikagél, illetve szerves polimer alapú hordozókra rögzített különféle funkcióscsoportok alkalmazása révén válnak alkalmassá az extrakció végrehajtására. Ilyenek például a C18, C8, C4, ciano-, amino-, diol-csoporttal módosított szilikagél, módosítatlan szilikagél, anion- és kationcserélők, vagy éppen különféle szennyezők meghatározásához fejlesztett speciális töltetek.
A szilárdfázisú extrakció térhódítását követően az 1990-es évek elején jelent meg az első olyan eszköz, amellyel lehetőség nyílt igen kicsiny mintatérfogatok (< 1 mL) reprodukálható extrakciójának elvégzésére is. A szilárdfázisú mikroextrakciót gáz és folyadék halmazállapotú minták extrakciójához tervezték kifejezetten úgy, hogy az extrakciót követően a minta közvetlenül adagolható legyen vagy gáz- vagy folyadékkromatográfba. (Az esetek túlnyomó többségében gázkromatográfiás meghatározásokhoz alkalmazzák a módszert.)
A szilárdfázisú mikroextrakció (solid phase microextraction, SPME) kivitelezésére tervezett fecskendő „lelke” egy extrakciós rudacska (vagy szál), ami a mechanikai sérülések elkerülése miatt egy hüvelyben helyezkedik el. Ebből egy egyszerű rugós mechanika segítségével kitolható, illetve oda visszahúzható a kb. 1 mm átmérőjű szál. Az extrakció műveletsorát az alábbi animáció mutatja be.
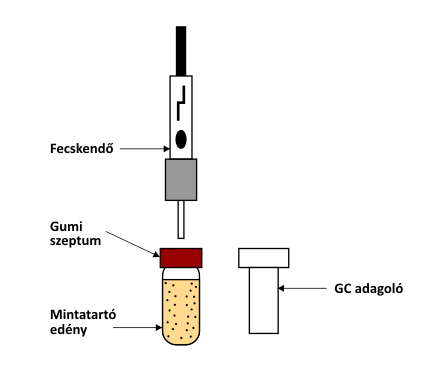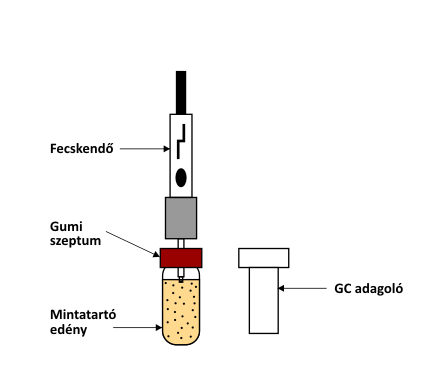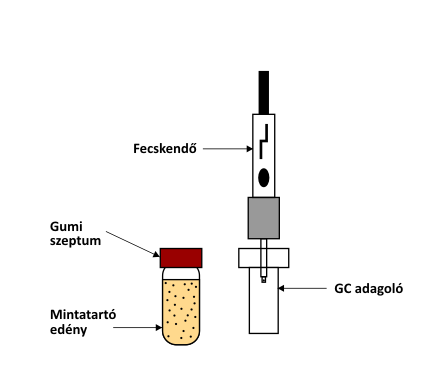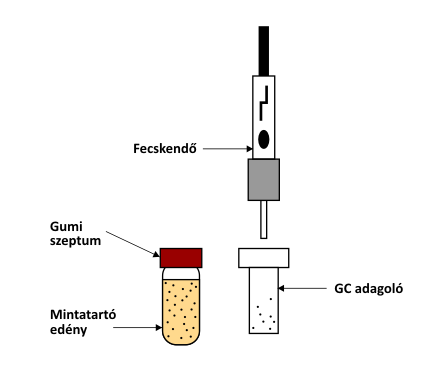
Az SPME extrakciós módszer műveletsora
A vizsgálandó mintát egy gázzáró, szeptummal ellátott mintartóedényben helyezik el. Az extrakció azzal kezdődik, hogy a lezárt mintatartó edény szeptumát át kell szúrni a fecskendővel (miközben az extrakciós szál visszahúzott állapotban van). Ezután a fecskendő dugattyújának lenyomásával és rögzítésével a hüvelyből kicsúszik a szál és elkezdődik az extrakció. A megfelelő extrakciós idő leteltével a dugattyú segítségével visszahúzzuk a szálat a hüvelybe, majd kihúzzuk fecskendőt a mintatartóból. Ezt követően a fecskendőt beszúrjuk a kromatográf adagolójába, majd a dugattyú lenyomásával és rögzítésével elkezdődik az extrahált minta deszorpciója, illetve kioldódása. Rövid várakozási időt követően visszahúzzuk a szálat a hüvelybe, majd kihúzzuk fecskendőt az adagolóból.
Az SPME „lelke” tehát az az extrakciós szál, tipikusan egy üveg rudacska, melynek felületére rögzítenek valamilyen filmet, vagy az üveg végére ragasztanak egy hasonlóan kicsiny méretű (1-2 cm hosszú, 1 mm-nél kisebb átmérőjű) adszorbenst. Abszorbensek esetén, az üvegrúdon rögzített megfelelő anyagi minőségű film fog extrahálószerként viselkedni, azaz magába oldja a mintát alkotó komponensek egy részét. Az egyik leggyakrabban használt bevonat a gázkromatográfiás kapilláris oszlopok megosztófázisaként is alkalmazott poli-dimetil-sziloxán (PDMS). A film vastagságának változtatásával változtatható az „extraháló szer” mennyisége. Minél vastagabb filmet alkalmazunk, annál nagyobb mennyiségű komponens extrakciója érhető el, de annál hosszabb extrakciós idő alkalmazása válik szükségessé. Napjainkban többféle (különböző polaritású) bevonattal ellátott extrakciós szál kapható kereskedelmi forgalomban, így mindig az extrahálni kívánt komponens(ek) anyagi minőségének (polaritásának) megfelelőt érdemes választani. Nemcsak abszorbenseket, hanem adszorbenseket, azaz porózus, nagy felülettel rendelkező anyagokat (pl. aktív szén) is lehet SPME céljára alkalmazni. Ezek lényegüket tekintve ugyanúgy működnek, mint bármely más művelet során alkalmazott adszorbens, azaz fizikai kölcsönhatásokon keresztül az adszorpciós kapacitásnak megfelelő mennyiségű komponens megkötésére képesek.
Összehasonlítva az SPE és az SPME módszerét elmondható, hogy az SPE a vizsgálandó komponens teljes kinyerésére törekszik (>90%) viszont az extraktumnak csak egy töredékét (1-2%) adagoljuk be a mérőberendezésbe. Ezzel ellentétben az SPME során csak töredékét extraháljuk a mérendő vegyületnek (1-20%), de az extraktum teljes egészét bejuttatjuk a mérőkészülékbe. További jelentős különbség a két módszer között az, hogy az SPME ellentétben az SPE-vel egyensúlyi (vagy legalábbis majdnem egyensúlyi) technika, ennek megfelelően minden olyan körülmény, ami beleszól az egyensúlyba (pH, hőmérséklet, sókoncentráció, térfogatok, extrakciós idő, stb.) hatással lesz az extrahált anyag mennyiségére.
Az SPME összevetve a többi extrakciós technikával számos előnnyel rendelkezik, többek között az alábbiakkal:
oldószermentes,
csak szorpciós és deszorpciós lépést tartalmaz,
könnyen automatizálható,
kompatibilis a kromatográfiás rendszerekkel,
nagy dúsítás érhető el,
a megfelelő specifikusság biztosítható,
nagyon kicsiny mintaigény jellemzi,
élő rendszerek vizsgálata is lehetséges,
a többszörös újrahasználhatóság miatt kifejezetten gazdaságosan alkalmazható.
A keverőrudas extrakciót (stirr bar sorptive extraction, SBSE) az 1990-es évek végén alkalmazták először kis koncentrációban jelenlevő szennyezők dúsítására. A módszer elvében megegyezik a korábban bemutatott SPME-vel. Kivitelezése igen egyszerű; egy megfelelő méretű (10-40 mm hosszú) mágneses keverőt az SPME-hez hasonló, de lényegesen vastagabb bevonattal (0,3-1 mm vastagságú PDMS réteg) látnak el, amint azt az alábbi ábra mutatja.
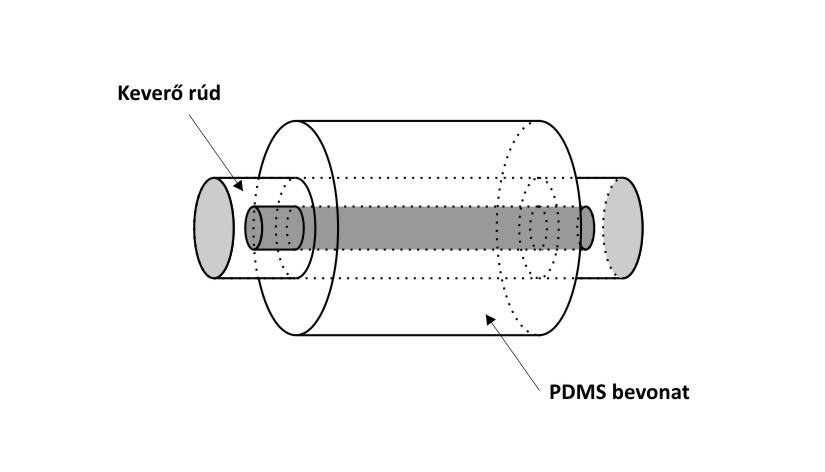
Keverőrudas (keverőbabás) extrakciós eszköz
Ezt a keverőrudat belehelyezik a minta oldatába, majd megfelelő ideig kevertetik az oldatot. Az oldatból kivéve a keverőrudat (amely immáron magába oldotta az analizálni kívánt komponensek egy részét), a kromatográfhoz kapcsolt vagy attól független egységben elhelyezve végrehajtható az extrahált komponensek eltávolítása. Erre gázkromatográfiás analízis esetén termikus deszorpciót alkalmaznak. Mivel a deszorpció nem megy végbe pillanatszerűen, így a gázkromatográfba történő adagolást megelőzően ún. kriofókuszálást is alkalmaznak, azaz kifagyasztják a deszorbeálódott komponenseket. Ezt követően igen gyors felfűtéssel már lehet biztosítani a megfelelő sebességű adagolást. Amennyiben folyadékkromatográfiásan végzik el az extrahált minta analízisét, ultrahanggal segített oldószeres leoldást lehet alkalmazni a megkötött komponensek eltávolítására.
Az SBSE előnye az SPME-vel szemben a számottevően nagyobb kinyerés, ami a lényegesen nagyobb térfogatú bevonatnak köszönhető. Ez eredményezi azt, hogy kisebb koncentrációban jelenlevő szennyezők dúsítására is alkalmas.
A módszert elsősorban élelmiszer, környezeti, illetve biológiai minták előkészítési műveleteként alkalmazzák.
Illékony szerves vegyületeknek (volatile organic compounds, VOCs) azokat a szerves anyagokat szokás nevezni, amelyek 20 °C-on mért gőznyomása legalább 0,1 Hgmm. A vegyületcsoport jelentőségét elsősorban az adja, hogy számos olyan környezeti szennyező sorolható közéjük, amelyeket a korábbi évtizedekben óriási mennyiségben állított elő és alkalmazott különböző célokra az emberiség. Legfontosabb képviselőik az ún. halogénezett szénhidrogének, amelyeknél a szénhidrogének egy vagy több hidrogénatomját halogénatom helyettesíti. Ezek a vegyületek sok-sok szerves vegyületet nagyon jól oldanak, inertek, kémiailag stabilak, olcsón előállíthatók, így alkalmazásuk mind a szerves kémiai laboratóriumi, mind az ipari gyakorlatban nagyon elterjedt. Sajnálatos módon a nagyvolumenű alkalmazás azt eredményezte, hogy ezek az illékony szerves vegyületek óriási mennyiségben kerültek ki a környezetbe, azonban a természetben lejátszódó folyamatok azokat csak nagyon lassan képesek lebontani. Ennek megfelelően kémiai analízisük kiemelt fontosságú
Illékonyságuk miatt a VOC-ok minőségi és mennyiségi meghatározására a gázkromatográfia a legalkalmasabb módszer. Ennek megfelelően az utóbbi évtizedekben olyan mintaelőkészítő eljárásokat dolgoztak ki, amelyek a vegyületcsoportra jellemző illékonyságot kihasználva lehetővé teszik a gázkromatográfiás analízis végrehajtását. Az esetek túlnyomó többségében a mintaelőkészítés során első lépésben biztosítják az illékony vegyületek gázfázisba (avagy gőztérbe) történő átjutását, majd második lépésben (amennyiben szükséges) megoldják a minta koncentrálását. A következőek során két ilyen mintaelőkészítési technikát ismertetünk röviden.
A statikus gőztér-extrakció (static headspace extraction, SHE) során a mintát – amely általában folyadék halmazállapotú – egy szeptumos gázzáró mintatartóban elhelyezve a minta gőzteréből végezzük el az analízist. Szilárd minta esetén aprítással, illetve őrléssel biztosítható az illékony komponensek gőztérbe történő kikerülése, illetve a szilárd minta feloldásával érhető el a gőztér és a minta közötti egyensúly gyorsabb beállása.
Amint az alábbi ábra mutatja, a tipikusan 1-20 mL mintát tartalmazó gázzáró, szeptumos mintatartót szabályozható hőmérsékletű folyadékfürdőben helyezik el, biztosítva ezzel a folyadékfázis és a gőztér közötti egyensúly reprodukálható kialakulását.
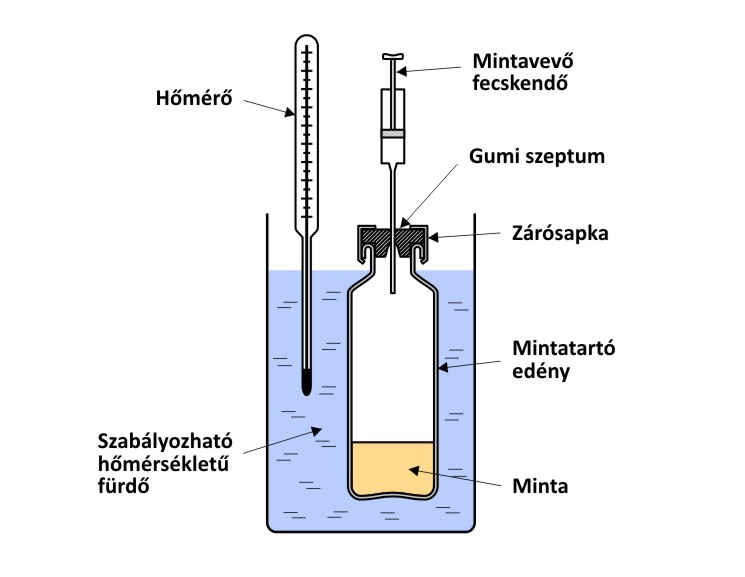
Az SHE extrakció kivitelezésének vázlata
Az egyensúly beálltával létrejön egy megoszlás a folyadék- és gázfázis között, azaz a mintát alkotó komponensek illékonyságuknak megfelelő mértékben kilépnek a gőztérbe. Természetesen minél nagyobb egy adott komponens illékonysága, annál nagyobb lesz a gőztérbeli koncentrációja. A szeptumot átszúrva, a gőztérből megfelelő térfogatú mintát kivéve elvégezhető a gázkromatográfiás elemzés. Amint az elmondottakból következik, az SHE egyensúlyi módszer, amely során részleges extrakciót hajtunk végre. A mintát alkotó komponensek gőztérbeli koncentrációjának alakulását minden olyan paraméter érinteni fogja, ami befolyásolja az egyensúly beállását (pl. nyomás, hőmérséklet, pH, stb.). Érthető módon tehát az egyensúlyt befolyásoló paraméterek megváltoztatásával nyílik lehetőség a gőztérbeli koncentráció viszonyok befolyásolására. Amennyiben szükséges mintaelőkészítés, az magában a mintatartó edényben elvégezhető, így az előkészítés és az analízis is könnyen automatizálható válik, azaz az SHE segítségével rövid idő alatt nagyszámú minta reprodukálható elemzése valósítható meg.
A dinamikus gőztér-extrakció (dynamic headspace extraction, DHE) abban különbözik a korábban bemutatott statikus gőztér-extrakciótól, hogy a meghatározandó (megfelelő illékonyságú) komponenseket folytonos gázátvezetéssel távolítják el a mintából, azaz ebben az esetben teljes extrakcióra törekszenek. A folyamatos gázátvezetés miatt koncentráció-gradiens alakul ki az öblítő gázban, ezért - illetve a megfelelő dúsítás és a pillanatszerű adagolás biztosítása miatt - a folyadék halmazállapotú mintán átbuborékoltatott gázt egy megfelelő minőségű és méretű csapdán vezetik át. A csapda segítségével megkötik az öblítőgáz által eltávolított komponenseket. A megkötött komponenseket a csapdáról pillanatszerűen eltávolítják és bejuttatják őket a gázkromatográfba. A DHE kialakítását az alábbi ábra szemlélteti.
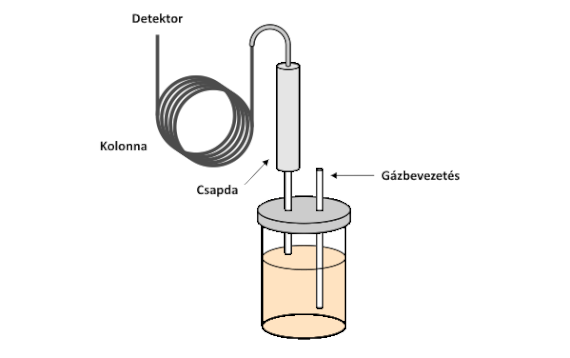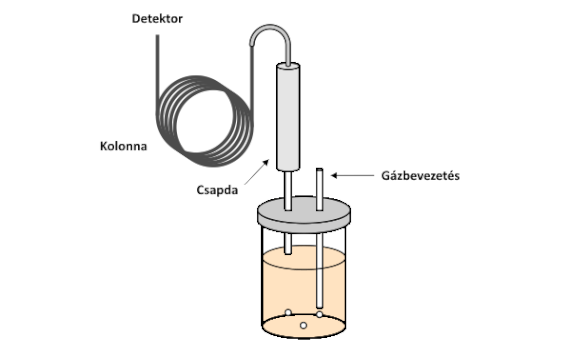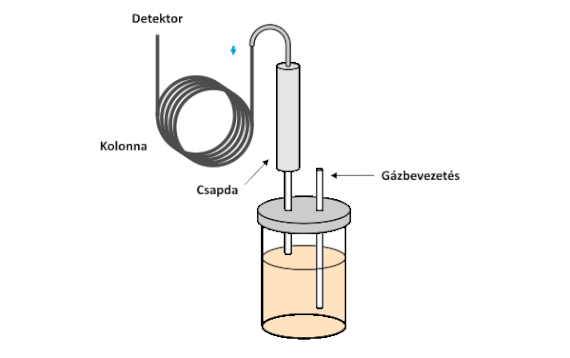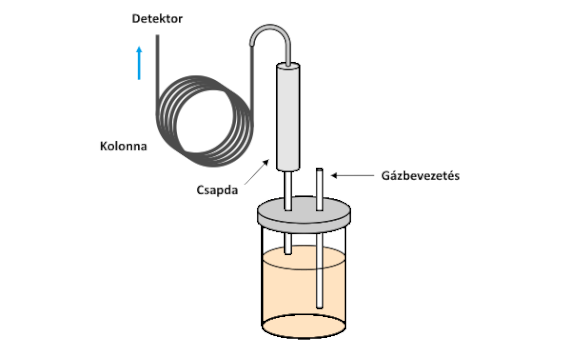
A DHE extrakció kivitelezésének vázlata
Csapdaként üveg vagy acél csőbe töltött különféle szorbensek jöhetnek szóba pl. az ún. Tenax, szilikagél vagy aktív szén (a Tenax kereskedelmi nevű anyag egy hidrofób tulajdonságú, pórusos 2,6-difenilén-oxid polimer gyanta, amely kb. 200 °C-os hőmérsékletig használható). Összetett rendszerek elemzéséhez célszerű réteges (kombinált) csapdát alkalmazni; a mintán átvezetett gáz először áthalad egy gyenge szorpciós tulajdonságokkal rendelkező tölteten (pl. Tenax), utána egy közepesen erős szorbensen (szilikagél), majd egy erős szorbens rétegen (aktív szén). Ennek a kialakításnak az az előnye, hogy a legerősebben kötődő (kevésbé illékony) komponensek már a gyengébb szorbensen megkötődnek, így a deszorpciójuk viszonylag könnyen kivitelezhető lesz. A dinamikus gőztér-extrakció általában az alábbi lépésekből áll:
öblítés: a mintán majd a csapdán is keresztülhalad az öblítőgáz, a csapdán megkötődnek az illékony összetevők,
száraz öblítés: célja az oldószer (víz) csapdáról történő eltávolítása: az öblítőgáz nem megy át a mintán, csak a csapdán,
előfűtés: felfűtjük a csapdát a deszorpció hőmérséklete alatti hőmérsékletre, ami gyorsítja a deszorpciót,
felfűtés: felfűtjük a csapdát a deszorpció hőmérsékletére (180-250 °C),
deszorpció: ellenirányú öblítőgáz átvezetésével eltávolítjuk a szorbensről a megkötött komponenseket (1-4 perc),
kriogén fókuszálás: amennyiben szükséges kifagyasztjuk a deszorbeálódott komponenseket,
adagolás,
szorbens regenerálása,
szorbens visszahűtése.
A dinamikus gőztér-analízis alkalmazására számos példa található (szilárd, illetve folyadék halmazállapotú) környezeti, biológiai, vagy ipari minták vizsgálata kapcsán.
Milyen célok elérését szolgálja az extrakció analitikai alkalmazása?
Milyen lépésekből áll a szilárdfázisú extrakció?
Milyen előnyökkel rendelkezik a szilárdfázisú extrakció a folyadék-folyadék extrakcióval szemben?
Milyen feltételeknek kell eleget tenniük a szilárdfázisú extrakció során alkalmazható szorbenseknek?
Ismertesse a szilárdfázisú mikroextrakció lépéseit!
Milyen előnyökkel rendelkezik a szilárdfázisú mikroextrakció?
Mit nevezünk keverőrudas extrakciónak?
Milyen komponensek meghatározására alkalmasak a gőztér-extrakción alapuló eljárások?
Miben hasonlítanak és miben különböznek a statikus és a dinamikus gőztér-extrakciós technikák?